
Заведующий лабораторией: член-корр. РАН, профессор Варфоломеев Сергей Дмитриевич
Телефон отдела: +7(499)137-64-20
Почта: sdvarf@sky.chph.ras.ru
Комната:—
Лаборатория кинетики и механизмов ферментативных и каталитических реакций, была создана в 1996 г. членом-корреспондентом РАН, д.х.н. Варфоломеевым С.Д. В составе лаборатории - 1 чл.-корр. РАН, 5 докторов наук, 13 кандидатов наук, младший научный персонал, инженеры-исследователи и аспиранты.

Коллектив лаборатории 0501
Основные сотрудники лаборатории – высококвалифицированные специалисты в области биоорганической и органической химии, кинетики и катализа ферментативных процессов, химической энзимологии, биофизики, микробиологии и нанотехнологий.
Научные исследования лаборатории проводятся в рамках двух научных тем ИБХФ РАН: «Физико-химические основы и принципы функционирования биологических макромолекул, регуляторных и надмолекулярных систем различной степени сложности; новые методы исследования, использование в современных высоких технологиях» и «Альтернативная энергетика и экология».
Научными партнерами лаборатории являются: кафедра химической энзимологии Химического факультета МГУ им. М.В. Ломоносова, Институт биоорганической химии им. академиков Шемякина М.М. и Овчинникова Ю.А. Российской академии наук, ФГБУ «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Минздрава РФ, Торакальное хирургическое отделение Московского научно-исследовательского онкологического института имени П.А. Герцена, ФГБУ «Научно-исследовательский институт пульмонологии Федерального медико-биологического агентства», ФГБУН «Государственный научный центр Российской Федерации Институт медико-биологических проблем Российской академии наук», ФГБУ "Научно-исследовательский испытательный центр подготовки космонавтов имени Ю.А. Гагарина", Кафедра госпитальной терапии Педиатрического факультета РНИМУ им. Н.И. Пирогова, Отделение клиники лучевых методов диагностики НИИ Неотложной детской хирургии и травматологии, кафедра биофизики Московский физико-технический институт (государственный университет), ФГБНУ Федеральный научный агроинженерный центр ВИМ, Федеральный исследовательский центр «Фундаментальные основы биотехнологии» Российской академии наук.
Ряд исследований лаборатории проводится в тесном сотрудничестве с другими лабораториями Института.
Основными направлениями исследований по научной теме 44.2 «Физико-химические основы и принципы функционирования биологических макромолекул, регуляторных и надмолекулярных систем различной степени сложности; новые методы исследования, использование в современных высоких технологиях» на 2025-2029 годы являются:
Проект «Исследование фотоники нового поколения гибридных диад, содержащих флуоресцентные и фотохромные метки» (отв. исполнитель – в.н.с., д.х.н. Ходонов А.А.)
Дизайн и разработка эффективных методов получения новых гибридных молекулярных структур и систем, содержащих фотохромные или флуорофорные фрагменты в качестве активных элементов, рабочие характеристики которых существенно изменяются под действием света с определенной длиной волны, представляют особый интерес для нужд бионанофотоники, фундаментальной медицины, фотофармакологии и биосенсорных технологий.
Особые перспективы для применения подобных систем отмечены при замене пока еще широко применяемых радиоактивных меток на более безопасные фотохромные, при разработке целого ряда прототипов технических smart-устройств в бионанофотонике и сенсорных технологиях и создании молекулярных оптических переключателей, для прототипов сенсорных устройств для детекции ионов, взрывчатых веществ и других лигандов, инфекционных агентов, для оценки протеолитической активности ферментных систем, для средств визуализации различных бионанообъектов в реальном времени и в многопараметрических (многоцветных) системах, для фотоуправляемых средств контроля строения и функции бионанообъектов (фотохромные сшивки, многопараметрические протоколы гибридизации нуклеиновых кислот; фотоуправляемые средства доставки биологически активных соединений и др.).

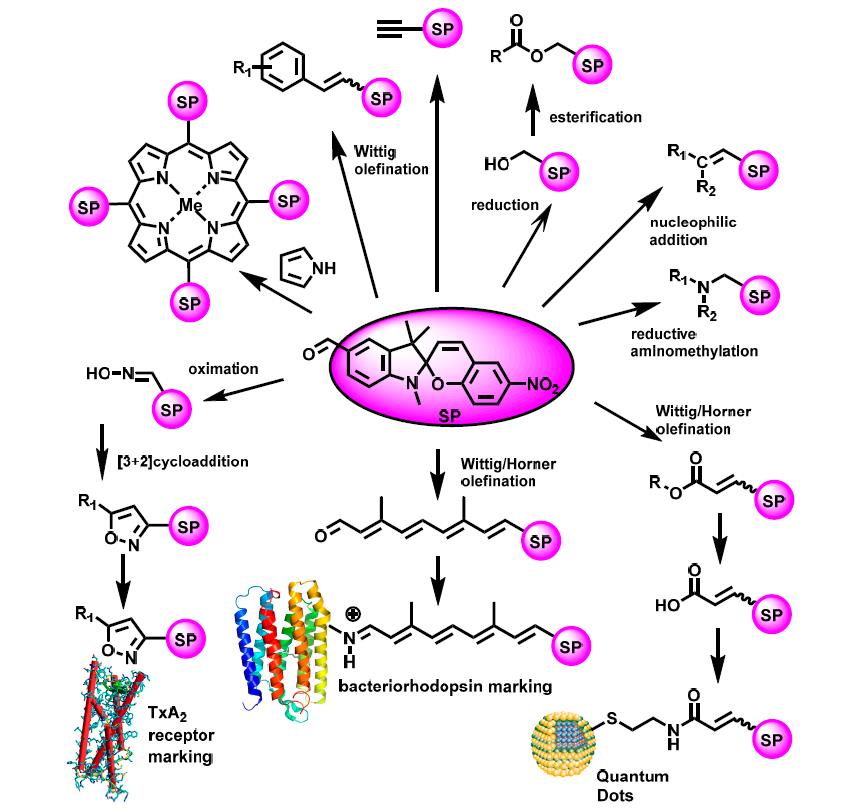
Основные тенденции в дизайне фотохромных зондов и меток

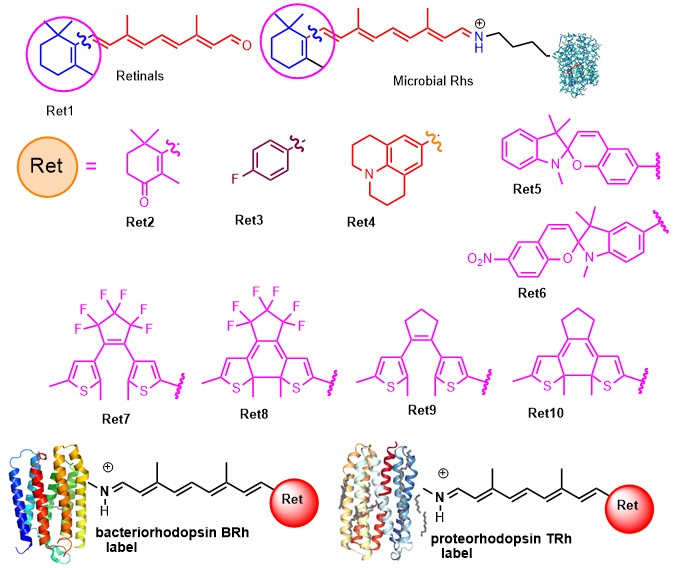
Структуры целевых фотоактивных лигандов - аналогов ретиналя
Проведеный нами анализ взаимосвязи структура хромофора - фотохимические свойства аналогов BRh позволил существенно расширить запланированную выборку наиболее перспективных структур аналогов ретиналя Ret2 - Ret10 для тестирования, и в результате этого были определены ключевые элементы структуры аналогов ретиналя, ответственные за связывание с белками–мишенями, и наличие определенных фотохимических свойств у образующихся аналогов BRh и TRh, с последующей разработкой и синтезом необходимого набора целевых изомеров и аналогов ретиноидов Ret2 - Ret10. Нами впервые были использованы фотохромные производные рядов спиропирана (Ret 5-6) и дитиенилэтенов (Ret 7-10) как фотохромно-меченные аналоги хромофорных групп у ряда микробных родопсинов. В результате проведенных исследований были определены структурные ограничения, накладываемые различными белковыми матрицами на строение молекулы хромофора и на фотохимические свойства искусственных пигментов BRh и TRh, и впервые была продемонстрирована возможность избирательного фоторегулирования процессом образования аналогов BRh из ретиналей Ret7 и Ret8.
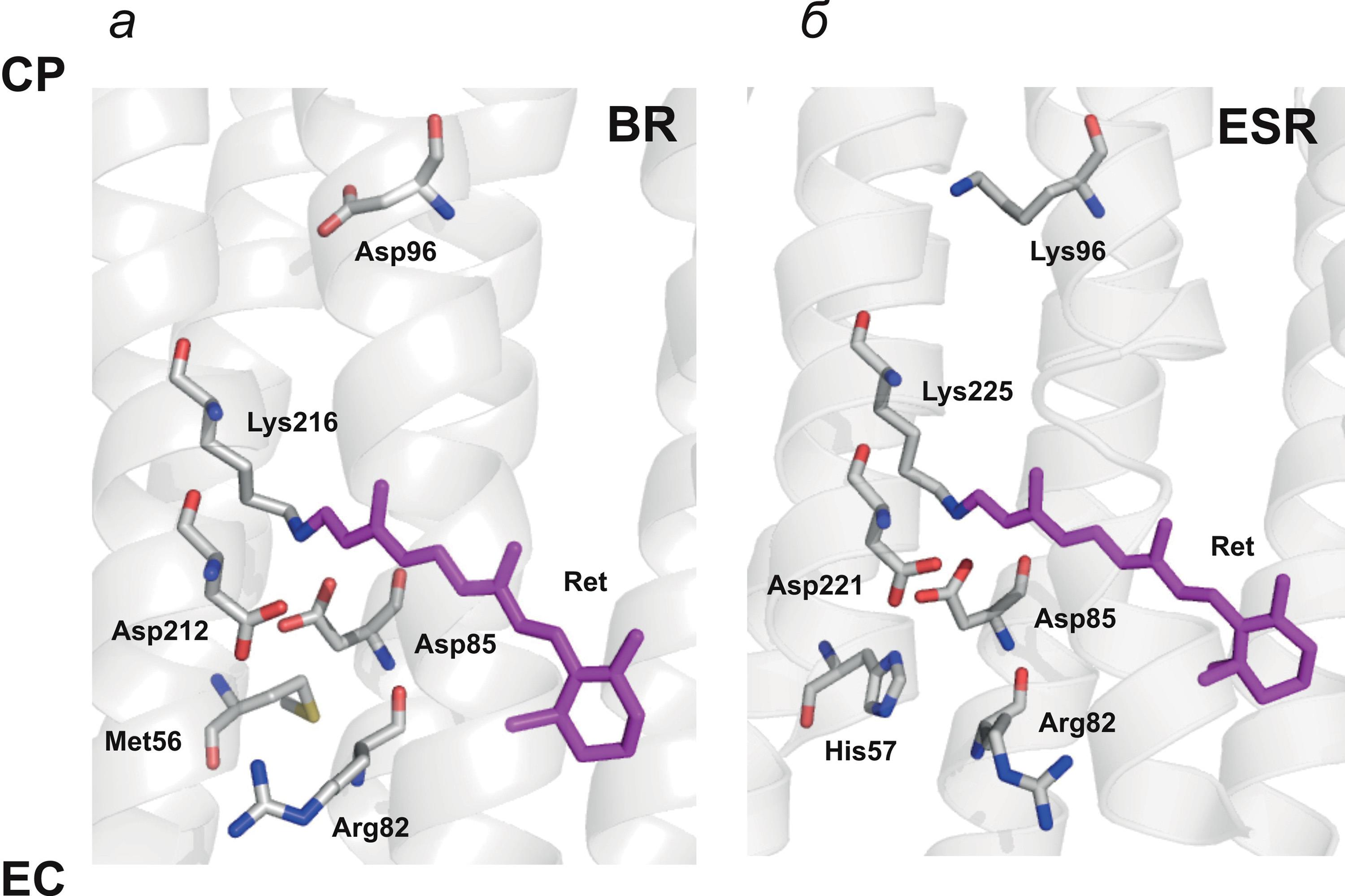
Была создана простая модель строения хромофорного центра, имитирующая влияние природы белкового микроокружения на оптические характеристики мишени в сайте связывания молекулы ретиналя в микробных родопсинах. Введение мощного электроно-донорного юлолидинового заместителя вместо триметилциклогексенового кольца природного хромофора (Ret1) в его модельном альдимине с н-бутиламином приводит к значительному увеличению величины λмакс основной полосы поглощения протонированного альдимина аналога ретиналя и его батохромного сдвига, Δλbatho) до значений (λмакс 592-597 нм и Δλbatho 162-167 нм).


В лаборатории была отработана технология получения модифицированных квантовых точек состава CdTe для ковалентной конъюгации с белками-мишенями; проведено комплексное исследование характеристик синтезированных флуоресцентных меток на их основе, включая флуоресцентные метки с «молекулярным адресом».
Проект «Дизайн, синтез и исследование потенциальных прототипов антитромбоцитарных средств с использованием линейки нативных индукторов агрегации» (отв. исполнитель – в.н.с., д.х.н. Дёмина О.В.)
Дизайн и синтез прототипов антитромбоцитарных средств с изучением их антиагрегационной активности и механизма действия – важная задача для сохранения здоровья людей, как в молодом, так и в зрелом возрасте.
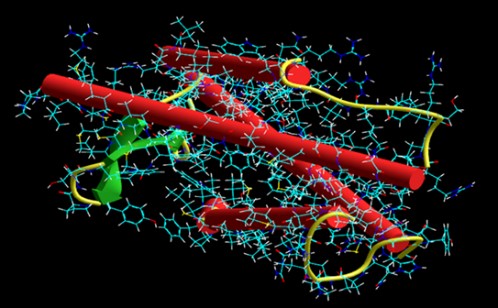
Первичная последовательность рецептора
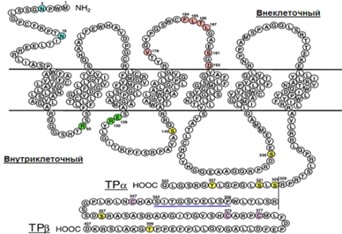
Рецептор тромбоксана А2
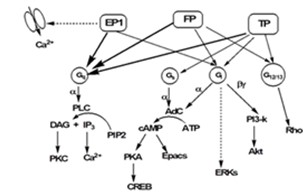
Пути передачи сигнала простаноидных рецепторов, сопряженных с G-белками
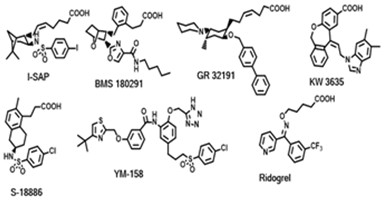
Антагонисты рецептора тромбоксана А2

Лазерный агрегометр «Биола»
В результате пандемии COVID-19 резко возрос интерес к эффектам аналогов простаноидов, тромбоксана А2 и простациклина, а также антагонистов рецепторов ADP, с возможным применением в комплексной терапии сердечно-сосудистых нарушений и заболеваний, даже при достаточно дорогостоящем синтезе. Это подтверждают многочисленные статьи по исследованию всех сигнальных путей простаноидов, так как до конца еще не изучены промежуточные стадии передачи сигнала, позволяющие его нивелировать в случае воспаления и ряда патологических процессов.
Ранее нами был разработан новый класс антиагрегационных средств - 5-замещенных 3-пиридилизоксазолов и их 4,5-дигидропроизводных c синтезом библиотек соединений и определением фармакофорного фрагмента, пространственных ограничений и механизма действия in vitro, разработаны методики получения отмытых тромбоцитов для лазерного агрегометра «Биола» и активации тромбоцитов малыми молекулами, исследованы кинетические закономерности процесса агрегации тромбоцитов человека под действием этих соединений, ряда их биоизостеров и позиционных изомеров с использованием линейки нативных индукторов агрегации; визуализировано взаимодействие веществ с мембранами тромбоцитов. Впервые показано наличие антитромбоцитарной активности для всех протестированных веществ при использовании арахидоновой кислоты, ADP и фактора активации тромбоцитов (PAF) как индукторов агрегации тромбоцитов человека. Впервые проведено сравнение влияния 3-(3-пиридил)-5-фенилизоксазола, его позиционного изомера и биоизостера на агрегацию тромбоцитов человека, вызванную миметиком тромбоксана А2 - U46619. Нами было доказано, что для дизайна антиагрегационных средств можно использовать основной скэффолд и 2 его модификации.
Отработанные нами методики агрегации и активации тромбоцитов человека позволяют проводить скрининг любых синтетических соединений.
Биологические исследования проводятся нами в рамках договора ИБХФ РАН с Федеральным государственным бюджетным учреждением «Национальный медицинский исследовательский центр детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева» Министерства здравоохранения Российской Федерации в сотрудничестве с лабораториями биофизики (зав. лаб. – д.б.н. Синауридзе Е.И.) и молекулярного гемостаза и тромбоза (зав. лаб. – чл.-корр. РАН, д.ф.-м.н. Пантелеев М.А.). Исследования были поддержаны 5 грантами РФФИ, по представленным результатам была получена медаль «Биотех-2011».
Проект «Исследование протеома конденсата выдыхаемого воздуха как метод неинвазивной диагностики состояния респираторной системы пациентов» (отв. исполнитель – с.н.с., к.х.н. Рябоконь А.М.)
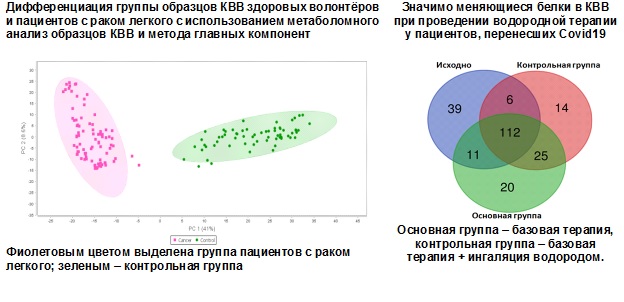
Одним из современных и перспективных направлений молекулярной биологии и медицины является разработка неинвазивных методов диагностики организма человека с выявлением биомаркеров - веществ, характеризующих наличие патологий, включая различные виды рака, в том числе и рак легкого. Анализ конденсата выдыхаемого воздуха (КВВ) является перспективным неинвазивным методом диагностики состояния респираторного тракта человека и может быть использован для мониторинга состояния здоровья групп населения, подверженных высокому риску развития различных патологий дыхательной системы, особенно раку легкого.
Использование в метаболомике и протеомике инновационных технологий - масс-спектрометрии ионного циклотронного резонанса с преобразованием Фурье, позволяет идентифицировать биомаркеры определенных заболеваний в КВВ. В рамках исследований была предложена панель из 105 метаболитов для диагностики рака легкого, разработан новый подход к обработке результатов масс-спектрометрического анализа конденсата выдыхаемого воздуха (КВВ) пациентов с раком легкого; показано, что совместный мониторинг характеристических маркеров и количественных изменений протеома повышает надежность и предсказательную способность анализа КВВ при раннем выявлении риска рака; предложена кинетическая модель развития коронавирусной инфекции; доказана высокая эффективность термогелиокса при COVID-19 и стимулировании иммунного ответа; впервые было исследовано более 50 проб конденсата выдыхаемого воздуха (КВВ) космонавтов после МКС с рекомендациями по реабилитации (совместно с лабораторией масс-спектрометрии биомакромолекул ИБХФ РАН и кафедрой госпитальной терапии Педиатрического факультета РНИМУ им. Н.М. Пирогова (акад. Чучалиным А.Г. и др.); разработан новый подход к обработке результатов масс-спектрометрического анализа конденсата выдыхаемого воздуха (КВВ) пациентов с раком легкого. Исследования были поддержаны 2 грантами РФФИ, 2 грантами РНФ и 3 раза поддержаны Программами Президиума РАН.
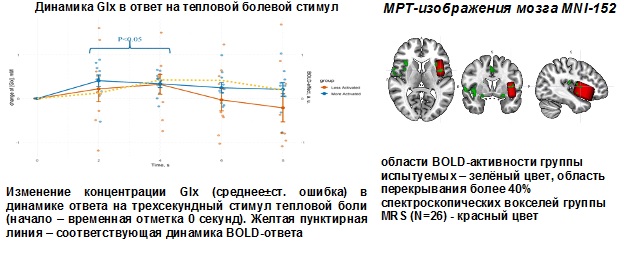
Проект «ЯМР-спектроскопия метаболитов центральной нервной системы человека: анализ влияния концентраций основных нейромедиаторов на параметры функции гемодинамического ответа на стимулы» (отв. исполнители – чл.-корр. РАН Варфоломеев С.Д., н.с., к.б.н. Ублинский М.В.)
Исследование механизмов действия механических и химических стимулов на головной мозг человека – одна из фундаментальных задач медицины и медицинской химии, позволяющая получить фундаментальные знания о функционировании мозга человека в норме и патологии, а также использовать полученные результаты для практического применения в клиниках. Магнитно-резонансная спектроскопия (МРС) пока единственный метод, позволяющий без повреждения организма человека оценить внутриклеточные концентрации ряда ключевых метаболитов за одно исследование.

До 2024 года данное направление исследований выполнялось под руководством гл.н.с., д.х.н. Семеновой Н.А.: была разработана методика редактирования локальных 1Н - ЯМР спектров мозга человека in vivo с неинвазивным определением концентраций основного тормозного нейромедиатора - гамма-аминомасляной кислоты (ГАМК), основного возбуждающего нейромедиатора – глутамата и их метаболитов; впервые было показано, что легкая МРТ- и КТ-негативная черепно-мозговая травма вызывает дисбаланс церебральных концентраций ГАМК и глутамата за счет роста концентрации ГАМК, показана динамика уровней концентраций этих веществ in vivo при видеостимуляции и динамике гемодинамического ответа (BOLD) на единичный стимул; было проведено изучение нарушения синтеза маркера функциональной активности нейронов N-ацетиласпартата (NAA) в мозге человека при черепно-мозговой травме, а также исследована прижизненная оценка эффектов гипербарической оксигенации на уровни фосфатных метаболитов в головном мозге человека. Впервые была разработана методика одновременного определения аспартата (Asp), глутамата (Glu) и NAA, основного предшественника синтеза N–ацетиласпартил-глутамата (NAAG), в локальных структурах мозга человека in vivo и проведено пилотное исследование влияния тяжелой черепно-мозговой травмы на содержание NAA, Asp и Glu в лобной доле мозга человека: полученные результаты свидетельствуют о ведущей роли малат-аспартатного шаттла в регуляции синтеза Asp и NAA на различных сроках после тяжелой черепно-мозговой травмы.
В настоящее время методом функциональной магнитно-резонансной томографии проводятся исследования выброса нейротрансмиттеров из везикул и их обратный захват при термальной и зрительной стимуляциях; выявлена активация в областях островковой коры с обоих сторон и дополнительной моторной коры головного мозга. Данное направление исследований было поддержано 2 грантами РНФ, 2 грантами РФФИ и Программой Президиума РАН. Все исследования проводятся на базе НИИ Неотложной Детской Хирургии и Травматологии г. Москвы.
Составной частью исследований при разработке прототипов лекарственных средств являются квантово-химические расчеты, используемые также для моделирования возможного механизма реакции фермент-субстрат, а также механизмов химических реакций и кинетических особенностей биологических процессов. Методы квантовой и молекулярной механики, используемые в этих исследованиях, уменьшают срок разработок и частично сокращают объем экспериментальной работы.
В результате успешного сотрудничества нашей лаборатории с лабораторией компьютерного моделирования биомолекулярных систем и наноматериалов (зав. лаб. – д.х.н., проф. А.В. Немухин (до августа 2023 года), с 2023 г. – к.ф-м.н. Поляков И.В.) и лаборатории химической кибернетики МГУ им. М.В. Ломоносова впервые методами молекулярного моделирования исследован полный каталитический цикл гидролиза N-ацетиласпартата ферментом человека аспартоацилазой (ASPA), одним из ключевых ферментов ЦНС, выполняющего гидролиз N-ацетиласпарагиновой кислоты (NAA). Структурные вариации фермента, отражающиеся на каталитической активности, связаны с рядом нейропатологий, прежде всего, с болезнью Канавана. Энергетические профили стадий химических превращений от фермент-субстратного комплекса до продукта были рассчитаны методами квантовой механики – молекулярной механики, профили входа субстрата и выхода продуктов – методами молекулярной динамики, с построением полной кинетической схемы многостадийного процесса, объясняющей экспериментальные исследования реакции, с получением детальной структурной информации. Результаты по компьютерному моделированию полного каталитического цикла аспартоацилазы были признаны важнейшими фундаментальными достижениями ИБХФ РАН 2016 года. В 2018 году важнейшим достижением Института стало компьютерное моделирование флуоресцентных белков (д.ф.-м.н. Б.Л. Григоренко, д.х.н. А.В. Немухин). Компьютерное моделирование строения, спектров и фотохимических свойств флуоресцентных белков было необходимо для прогнозирования новых, более эффективных биомолекулярных меток. По результатам суперкомпьютерных расчетов методами квантовой химии и молекулярной динамики установлены механизмы формирования хромофоров во флуоресцентных белках и охарактеризованы структуры и спектры нового класса маркеров – инфракрасных флуоресцентных белков на основе фитохромов. Для ряда ферментов был проведен поиск эффективных ингибиторов и/или активаторов с использованием компьютерного докинга синтетических веществ различной химической природы.
На данный момент проведено кинетическое моделирование и анализ закономерностей образования макрочастиц металлического золота и механизма образования макрочастиц металла, в результате - предложена кинетическая модель, описывающая процесс формирования металлического золота в теле техногенного минерального образования. Рассмотрены закономерности процесса в водном потоке с использованием химических механизмов взаимопревращений различных состояний золота, включая промежуточное образование коллоидных частиц. На основании предложенной модели дано объяснение экспериментальному факту накопления металлического золота в результате “химической эволюции” системы на различных глубинах искусственного минерального образования. В рамках кинетической модели проведен анализ влияния на поведение системы концентраций восстанавливающих агентов, интенсивности эрозии золотосодержащих минералов, содержания “рассеянного” коллоидного золота. (отв. – чл.-корр. РАН Варфоломеев С.Д., в.н.с., д.ф.-м.н. Цыбенова С.Б., в.н.с., д.ф.-м.н. Быков В.И.)
Проведено моделирование различных комплексов белок-лиганд методами КМ/ММ, по результатам которого был разработан универсальный критерий для определения механизма расщепления связи P–O в ферментах (ассоциативный или диссоциативный) без трудоёмкого расчёта полного энергетического профиля реакции. Критерий проверен на 15 ферментах и подтверждён расчётами для аденилаткиназ, показав высокую надёжность и значительную экономию вычислительных ресурсов. (отв. - в.н.с., д.ф.-м.н. Хренова М.Г., зав. лаб., к.ф.-м.н. Поляков И.В.).
Проводимые исследования демонстрируют эффективность современных вычислительных методов для решения актуальных научных и практических задач химии. Применение кинетического моделирования, методов молекулярной динамики и квантово-химических расчётов позволило добиться значимых результатов в различных областях: от моделирования процессов образования металлов до углублённого анализа механизмов ферментативных реакций. Таким образом, использование комплекса методов математического и молекулярного моделирования служит мощным инструментом, который сокращает время и затраты на фундаментальные исследования и прикладные разработки. Это направление является чрезвычайно перспективным для создания новых поколений лекарственных препаратов и функциональных материалов.
Проект «Разработка биокаталитических процессов трансформации синтетических полимеров для решения задач энергосбережения и/или альтернативной энергетики» (отв. исполнитель – с.н.с., д.б.н. Ефременко Е.Н.)

Разработка биокаталитических процессов, направленных на трансформацию синтетических полимеров с целью решения задач энергосбережения и/или альтернативной энергетики является важным направлением науки, совмещающим фундаментальные исследования в области создания недорогих биокатализаторов с долгим сроком функционирования и практическое использование этих знаний при переработке растительного вторсырья и синтетических полимеров, получения биотоплива и биогаза. В нашей лаборатории такие работы проводятся совместно с кафедрой химической энзимологии Химического факультета и кафедрой биотехнологии МГУ им. М.В. Ломоносова и Федеральным государственным бюджетным научным учреждением Федеральный научный агроинженерный центр ВИМ (ФНАЦ ВИМ, Москва).
Ранее этим коллективом был выполнен ряд проектов по получению полупродуктов для биотоплив из ряда отходов сельского хозяйства и микроводорослей, включая проект «Разработка методов получения биотоплива на основе микробиологических подходов, включая переработку органических материалов» совместно с кафедрой химической энзимологии Химического факультета МГУ им. М.В. Ломоносова, так как данное направление исследований очень актуально для мировой прикладной науки. В лаборатории впервые были разработаны высокоэффективные биокатализаторы в виде иммобилизованных в криогель поливинилового спирта клеток анаэробных консорциумов для конверсии в метан различных субстратов: отходов сельского хозяйства (гидролизатов стеблей топинамбура, свекловичного жома, багассы), отходов перерабатывающей промышленности (древесные опилки, стоки молокозавода). Была показана универсальность разработанного способа получения подобных биокатализаторов (массовое соотношение компонентов биокатализаторов, физико-химические характеристики применяемых сред и процесса иммобилизации) на примере разных по составу метаногенных анаэробных консорциумов. Была продемонстрирована возможность длительного функционирования полученных биокаталитических систем со стабильными характеристиками по конверсии различных исходных субстратов.
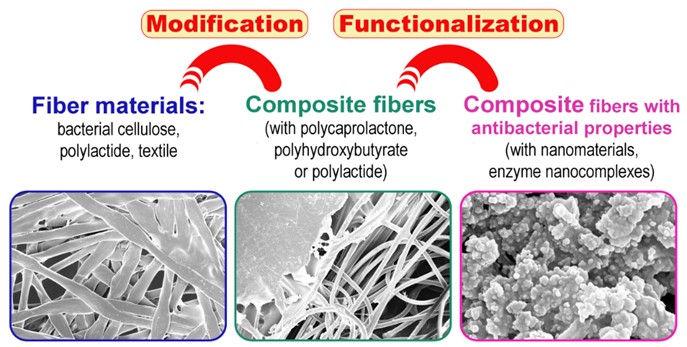
На основании ранее полученных результатов был научно обоснован комплексный подход к трансформации отработанных синтетических полимеров с использованием разных биокатализаторов и/или их комбинаций. Были разработаны и модифицируются методы получения иммобилизованных полиферментных систем - клеток разных микроорганизмов, методы их исследования и использования в высоких технологиях переработки органических материалов. Установлены характеристики полимеров и методы их функционализации, негативно влияющие на активность ферментов иммобилизованных микроорганизмов, установлены основные сайты воздействия в бактериальных биокатализаторах. Предложен двухстадийный процесс переработки отходов поликапролактона, соответствующий всем требованиям современных экологических стандартов безопасности и ресурсосбережения.
Данные исследования поддержаны 4 грантами РФФИ и 1 международным грантом РФФИ, 2 грантами РНФ, 5 Программами Президиума РАН, Программой ОХНМ РАН , 1 госконтракт ФЦП. Результаты были представлены на 4-х выставках, вручена золотая медаль «Архимед-2016».
В последние годы очень актуальным является решению двух неразрывно связанных проблем – предотвращения истощения природных ресурсов и охране окружающей среды от загрязнения. Быстрое расходование запасов природного топлива, ограничение строительства гидро- и атомных электростанций вызвали интерес к применению возобновляемых источников энергии, в том числе огромных масс органических отходов, образующихся в сельском хозяйстве, промышленности, городском коммунальном хозяйстве. В связи с этим использование методов биологической конверсии органических отходов с получением биогаза и высококачественных органических удобрений при одновременном решении ряда вопросов охраны окружающей среды от загрязнения является весьма перспективным.
На данный момент по теме работы выполнен анализа текущей литературы с обзором способов получения реагентов для физико-химического кондиционирования биогаза. На основании обзора промышленных методов была разработана принципиальная схема экспериментальной установки комбинированного физико-химического кондиционирования биогаза, проведены расчеты поверхности отклика стехиометрического расхода промывочного раствора от переменных - концентраций углекислого газа в биогазе и промывочного раствора с использованием ПО “DesignExpert “. Планируется создание экспериментальной установки для кондиционирования биогаза включающей блок приготовления реагента (электролизер), мокрый скруббер для промывки биогаза, химический реактор для взаимодействия карбоната натрия и хлорноватистой кислоты, получаемой в процессе электролиза раствора хлорида натрия. Разрабатываемый способ кондиционирования биогаза позволит получать биометан с содержанием до 96% для применения в газоиспользующем оборудовании (котлы, ГПУ, ГТУ).
Основным направлением работы являются теоретические исследования (моделирование) в области химической и биологической кинетики, включая кинетику многостадийных последовательных и разветвленных ферментативных реакций, популяционную динамику, кинетику фазовых переходов. Особый интерес представляет формирование устойчивых и неустойчивых стационарных состояний при протекании химических реакций, а также биофизическая/биохимическая интерпретация результатов моделирования.
В настоящее время в результате исследования математической модели фазового перехода обнаружено существование двух устойчивых стационарных состояний, соответствующих разным температурам, и высокая чувствительность системы к внешним условиям вблизи фазового перехода. Рассмотрена гипотеза о роли фазовых переходов в ходе пребиологической эволюции макромолекул: фазовые переходы I рода в среде, где происходит эволюция молекул, могут быть ключевым условием возникновения жизни. Показано, что в нескольких устойчивых состояниях стабильными являются разные формы нуклеиновых кислот (димер и мономер), из которых только одна (мономер) обладает каталитической активностью. (н.с., к.ф.-м.н. Луковенков А.В.)
Проведен анализ литературных данных по перекрестному взаимодействию метаболических систем с проводящими сигнал каскадами, активируемыми нейротрансмиттерами в астроцитах. Предложена блок-схема инициирования BOLD сигнала возбуждающими и модулирующими нейротрансмиттерами посредством волны внутриклеточного кальция с последующей активацией гликолиза в астроцитах и окислительного фосфорилирования в нейронах. Полученные результаты можно использовать для изучения молекулярно-кинетических механизмов физиологических и патологических процессов в ЦНС по динамике изменения BOLD сигнала и параметров метаболизма и внутриклеточной сигнализации (креатинфосфата, NAA, АТФ, лактата, инозитола и др.). (с.н.с., к.б.н. Сухомлин Т.К.)
Исследования необходимы для планирования дальнейших работ в области фундаментальной и практической медицины, нейробиологии и биофизики.

За период 1997 – 2025 гг. сотрудники лаборатории участвовали более чем в 500 всероссийских и международных конференциях, съездах и симпозиумах, было опубликовано более 750 тезисов докладов, сделано более 360 устных докладов.
За это время были успешно защищены 2 докторские диссертации и 14 кандидатских диссертаций. За 1997-2025 гг. были выполнены 3 международные программы, 15 проектов по Программам Президиума РАН, 1 Госконтракт ФЦНТП 2002-2006 гг., 1 Госконтракт ФЦП 2011-2012 гг., 2 Программы ОХМН Президиума РАН, 1 Программа МГУ (18 договоров), 25 грантов РФФИ, 1 грант РНФ.


Помощником С.Д. Варфоломеева - к.б.н. Найдич В.И., была проведена большая организаторская и редакторская работа по подготовке к изданию ряда книг, монографий, учебников и сборников статей.